W wyniku pewnej odwracalnej reakcji chemicznej z dwóch substratów powstaje jeden produkt. Przemiana przebiega w fazie gazowej, co oznacza, że oba substraty i produkt są gazami. Reakcję tę przeprowadzono w zamkniętym reaktorze przy użyciu stechiometrycznych ilości substratów w różnych temperaturach i pod różnym ciśnieniem. Na poniższym diagramie przedstawiono, jaki procent objętości mieszaniny poreakcyjnej w reaktorze stanowiła objętość produktu tej reakcji w zależności od warunków temperatury i ciśnienia, w jakich przebiegała.
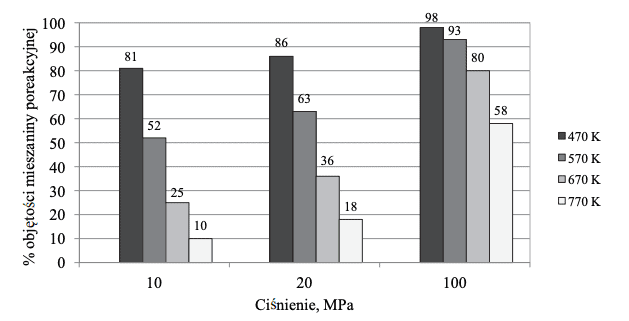
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2010.
Na podstawie analizy diagramu określ, czy w czasie opisanej reakcji układ oddaje energię do otoczenia, czy przyjmuje ją od otoczenia. Odpowiedź uzasadnij.
……………………………………………………………………………………………………..

Odpowiedzi
Czy w tym zadaniu w uzasadnieniu można napisać, że ze wzrostem temp spada wydajność bez dodawania informacji o regule przekory?
Hej! To nie wystarczy, bo tak naprawdę to jest nadal opisanie zależności, a nie jej wyjaśnienie 🙂 Taka wskazówka do tego typu zadań – wyjaśniamy zwykle poprzez prawa chemiczne, budowę związku lub atomu.