Zadania maturalne z chemii
Zadanie 30. CKE Maj 2017 PR (formuła 2015-2022)
Poniżej przedstawiono wzory: cykloheksanonu, cykloheksanolu i kwasu adypinowego. Literami a, b i c oznaczono wybrane atomy węgla.

Określ formalne stopnie utlenienia oraz typ hybrydyzacji (sp, sp2, sp3) atomów węgla oznaczonych w podanych wzorach literami a, b i c. Uzupełnij tabelę.
| Atom węgla | w cykloheksanonie | w cykloheksanolu | w kwasie adypinowym |
|---|---|---|---|
| a | b | c | |
| Stopień utlenienia | |||
| Typ hybrydyzacji |
Schemat punktowania
2 p. – za poprawne uzupełnienie dwóch wierszy tabeli.
1 p. – za poprawne uzupełnienie jednego wiersza tabeli.
0 p. – za odpowiedź niepełną lub błędną albo brak odpowiedzi.
Poprawna odpowiedź
| Atom węgla | w cykloheksanonie | w cykloheksanolu | w kwasie adypinowym |
|---|---|---|---|
| a | b | c | |
| Stopień utlenienia | II | 0 | III |
| Typ hybrydyzacji | sp2 | sp3 | sp2 |
Zadanie 6. CKE Maj 2017 PR (formuła do 2015)
W poniższej tabeli zestawiono wybrane właściwości pewnej substancji.
| masa molowa | 42 g·mol–1 |
| temperatura topnienia pod ciśnieniem 1013 hPa | 610°C |
| temperatura wrzenia pod ciśnieniem 1013 hPa | 1360°C |
| rozpuszczalność w wodzie w temperaturze 20°C | 84 g w 100 g H2O |
| przewodnictwo elektryczności w ciekłym stanie skupienia | tak |
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 1997.
Wybierz i podkreśl w każdym nawiasie poprawne uzupełnienie poniższych zdań.
Opisana substancja jest związkiem (jonowym / kowalencyjnym). W wodzie występuje w postaci (niezdysocjowanej / zdysocjowanej), dlatego jej wodny roztwór (przewodzi prąd elektryczny / nie przewodzi prądu elektrycznego).
Schemat punktowania
1 p. – za poprawne uzupełnienie obu zdań.
0 p. – za odpowiedź niepełną lub błędną albo brak odpowiedzi.
Poprawna odpowiedź
Opisana substancja jest związkiem (jonowym / kowalencyjnym). W wodzie występuje w postaci (niezdysocjowanej / zdysocjowanej), dlatego jej wodny roztwór (przewodzi prąd elektryczny / nie przewodzi prądu elektrycznego).
Zadanie 34. CKE Maj 2018 PR (formuła 2015-2022)
Aktywne formy witaminy D, odgrywające ważną rolę w kontrolowaniu metabolizmu wapnia i fosforu, nie występują w pokarmie. Pod wpływem światła słonecznego obie aktywne formy są wytwarzane pod powierzchnią skóry w wyniku różnych przemian, np. reakcji fotochemicznej, reakcji polegającej na otwarciu pierścienia, izomeryzacji, a także przemian metabolicznych, np.:

Na podstawie: J. McMurry, Chemia organiczna, Warszawa 2000 oraz J. Berg, J. Tymoczko, L. Stryer, Biochemia, Warszawa 2007.
Podaj nazwę grup funkcyjnych, których wprowadzenie do szkieletu cząsteczki witaminy D3 skutkuje przekształceniem witaminy w jej aktywną formę. Określ formalne stopnie utlenienia atomów węgla oznaczonych w powyższym wzorze literami a i b oraz określ hybrydyzację orbitali walencyjnych atomów węgla oznaczonych tymi samymi literami. Uzupełnij tabelę.
Nazwa: …………………………………………………………………………..
| atom węgla | a | b |
| stopień utlenienia węgla | ||
| hybrydyzacja węgla |
Schemat punktowania
1 p. – za poprawne podanie nazwy grup funkcyjnych i poprawne uzupełnienie tabeli.
0 p. – za każdą inną odpowiedź albo brak odpowiedzi.
Poprawna odpowiedź
Nazwa: (grupy) hydroksylowe lub (grupy) wodorotlenowe
| atom węgla | a | b |
| stopień utlenienia węgla | 0 | I |
| hybrydyzacja węgla | sp3 | sp3 |
Zadanie 29. CKE Maj 2018 PR (formuła 2015-2022)
Chlorowcopochodne alkanów reagują z metalicznym litem, w wyniku czego tworzą związki litoorganiczne (których wzór w uproszczeniu można zapisać jako RLi). Reakcja przebiega
zgodnie ze schematem:
RX +2Li → RLi + LiX
Związki litoorganiczne gwałtownie reagują z wodą z wydzieleniem wolnego węglowodoru. Roztwór po takiej reakcji ma odczyn zasadowy. W reakcjach związków litoorganicznych
z jodkiem miedzi(I) powstaje związek miedziolitoorganiczny R2CuLi zgodnie z poniższym schematem:
2RLi + CuI → R2CuLi + LiI
Związek R2CuLi jest zwany odczynnikiem Gilmana. Ten odczynnik może reagować z inną chlorowcopochodną, w wyniku czego tworzy odpowiedni węglowodór (R–R’), co zilustrowano
schematem:
R2CuLi + R’X → R–R’ + LiX + RCu
Na podstawie: J. McMurry, Chemia organiczna, Warszawa 2000.
Temperatura topnienia butylolitu (C4H9Li) jest znacznie niższa od 0°C.
Na podstawie różnicy elektroujemności między litem a węglem oraz informacji wprowadzającej dotyczącej temperatury topnienia butylolitu określ rodzaj wiązania węgiel – lit.
………………………………………………………………………………………………………………………
Schemat punktowania
1 p. – za poprawne określenie rodzaju wiązania.
0 p. – za każdą inną odpowiedź albo brak odpowiedzi.
Poprawna odpowiedź
kowalencyjne spolaryzowane lub atomowe spolaryzowane lub kowalencyjne lub atomowe
Zadanie 27. CKE Maj 2018 PR (formuła 2015-2022)
W poniższej tabeli zestawiono informacje na temat cząsteczek trzech węglowodorów o prostych (nierozgałęzionych) łańcuchach węglowych.
| Węglowodór | Liczba atomów węgla o danej hybrydyzacji | Dodatkowe informacje | ||
| sp | sp2 | sp3 | ||
| A | 0 | 4 | 0 | brak |
| B | 0 | 2 | 2 | występuje w postaci izomerów cis i trans |
| C | 2 | 0 | 2 | dwa atomy węgla w cząsteczce nie są związane z atomami wodoru |
Przeprowadzono reakcję węglowodoru C z wodą w stosunku molowym nwęglowodoru C : nH2O = 1:1.
Napisz wzór półstrukturalny (grupowy) trwałego (dominującego) produktu reakcji, której substratami są węglowodór C i woda.
……………………………………………………………………………………………………..
Schemat punktowania
1 p. – za poprawnie zapisanie wzoru związku.
0 p. – za błędną odpowiedź albo brak odpowiedzi.
Poprawna odpowiedź

Zadanie 26. CKE Maj 2018 PR (formuła 2015-2022)
W poniższej tabeli zestawiono informacje na temat cząsteczek trzech węglowodorów o prostych (nierozgałęzionych) łańcuchach węglowych.
| Węglowodór | Liczba atomów węgla o danej hybrydyzacji | Dodatkowe informacje | ||
| sp | sp2 | sp3 | ||
| A | 0 | 4 | 0 | brak |
| B | 0 | 2 | 2 | występuje w postaci izomerów cis i trans |
| C | 2 | 0 | 2 | dwa atomy węgla w cząsteczce nie są związane z atomami wodoru |
Narysuj wzór półstrukturalny (grupowy) izomeru cis węglowodoru B.
Schemat punktowania
1 p. – za poprawnie zapisanie wzoru izomeru cis związku.
0 p. – za błędną odpowiedź albo brak odpowiedzi.
Poprawna odpowiedź

Zadanie 25. CKE Maj 2018 PR (formuła 2015-2022)
W poniższej tabeli zestawiono informacje na temat cząsteczek trzech węglowodorów o prostych (nierozgałęzionych) łańcuchach węglowych.
| Węglowodór | Liczba atomów węgla o danej hybrydyzacji | Dodatkowe informacje | ||
| sp | sp2 | sp3 | ||
| A | 0 | 4 | 0 | brak |
| B | 0 | 2 | 2 | występuje w postaci izomerów cis i trans |
| C | 2 | 0 | 2 | dwa atomy węgla w cząsteczce nie są związane z atomami wodoru |
Przeprowadzono reakcję węglowodoru A z wodorem, w której stosunek molowy węglowodoru do wodoru był równy nwęglowodoru A : nH2 = 1 : 2.
Napisz równanie reakcji węglowodoru A z wodorem. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.
……………………………………………………………………………………………………..
Schemat punktowania
1 p. – za poprawnie napisanie równania reakcji.
0 p. – za błędne napisanie równania reakcji (błędne wzory reagentów, błędne współczynniki stechiometryczne, niewłaściwa forma zapisu) albo brak odpowiedzi.
Poprawna odpowiedź
H2C=CH-CH=CH2 + 2H2 → H3C-CH2-CH2-CH3
Uwaga! Określenie warunków reakcji nie podlega ocenie.
Zadanie 1. CKE Maj 2018 PR (formuła 2015-2022)
Pierwiastki X i Z leżą w czwartym okresie układu okresowego. Pierwiastek X jest metalem, natomiast pierwiastek Z niemetalem. W stanie podstawowym atomów obu tych pierwiastków tylko jeden elektron jest niesparowany. Znajduje się on na ostatniej powłoce. Niesparowany elektron atomu pierwiastka X znajduje się na innej podpowłoce niż niesparowany elektron atomu pierwiastka Z. Ponadto wiadomo, że pierwiastek X tworzy tlenki o wzorach X2O i XO oraz że ten metal jest jednym z najlepszych przewodników ciepła i elektryczności. Pierwiastek Z występuje w postaci dwuatomowych cząsteczek.
1.1.
Uzupełnij poniższą tabelę. Wpisz symbole pierwiastków X i Z, dane dotyczące ich położenia w układzie okresowym oraz symbol bloku konfiguracyjnego, do którego należy każdy z pierwiastków.
| Symbol pierwiastka | Numer grupy | Symbol bloku | |
|---|---|---|---|
| pierwiastek X | |||
| pierwiastek Z |
1.2.
Przedstaw konfigurację elektronową jonu X2+ (stan podstawowy). Zastosuj skrócony zapis konfiguracji elektronowej z symbolem gazu szlachetnego.
……………………………………………………………………………………………………..
1.3.
Dla cząsteczki Z2 określ liczbę: wiązań σ, wiązań π oraz wolnych par elektronowych.
| Liczba | ||
|---|---|---|
| wiązań σ | wiązań π | wolnych par elektronowych |
1.1. (0–1)
Schemat punktowania
1 p. – za poprawne uzupełnienie wszystkich komórek tabeli.
0 p. – za odpowiedź niepełną lub błędną albo brak odpowiedzi.
Poprawna odpowiedź
| Symbol pierwiastka | Numer grupy | Symbol bloku | |
|---|---|---|---|
| pierwiastek X | Cu | 11 | d |
| pierwiastek Z | Br | 17 | p |
1.2. (0–1)
Schemat punktowania
1 p. – za poprawne napisanie skróconej (z zastosowaniem symbolu argonu) konfiguracji elektronowej jonu Cu2+.
0 p. – za odpowiedź błędną albo brak odpowiedzi.
Poprawna odpowiedź
[Ar] 3d9lub

Uwaga! Zastosowanie zapisu klatkowego bez uwzględnienia numeru powłoki lub symbolu podpowłoki powoduje utratę punktu.
1.3. (0–1)
Schemat punktowania
1 p. – za poprawne podanie liczby wiązań σ i π oraz wolnych par elektronowych w cząsteczce Br2.
0 p. – za odpowiedź niepełną lub błędną albo brak odpowiedzi.
Poprawna odpowiedź
| Liczba | ||
|---|---|---|
| wiązań σ | wiązań π | wolnych par elektronowych |
| 1 | 0 | 6 |
Zadanie 26. CKE Czerwiec 2019 PR (formuła 2015-2022)
Ubichinon Q10 (koenzym Q10) jest niezbędnym elementem łańcucha oddechowego. Zapobiega produkcji rodników, oksydacyjnym modyfikacjom białek, lipidów oraz DNA i pełni wiele innych funkcji w organizmie. Poniżej przedstawiono wzór opisujący strukturę cząsteczki ubichinonu Q10.
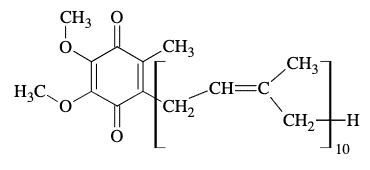
Oceń, czy poniższe informacje są prawdziwe. Zaznacz P, jeśli informacja jest prawdziwa, albo F – jeśli jest fałszywa.
| 1. | Cząsteczka ubichinonu Q10 o strukturze przedstawionej w informacji zawiera 14 wiązań π. | P | F |
| 2. | Cząsteczka ubichinonu Q10 o strukturze przedstawionej w informacji zawiera pierścień aromatyczny. | P | F |
| 3. | W łańcuchowym fragmencie cząsteczki ubichinonu Q10 o strukturze przedstawionej w informacji wszystkim atomom węgla można przypisać hybrydyzację sp2 | P | F |
Schemat punktowania
1 p. – za poprawne wskazanie trzech odpowiedzi.
0 p. – za odpowiedź niepełną lub niepoprawną albo brak odpowiedzi.
Poprawna odpowiedź
1 – P, 2 – F, 3 – F
Zadanie 23. CKE Maj 2019 PR (formuła 2015-2022)
Jedną z metod otrzymywania halogenoalkanów jest reakcja alkoholu alifatycznego z halogenkiem fosforu(III). Ta reakcja przebiega zgodnie z poniższym schematem, w którym R oznacza grupę alkilową, a X – atom halogenu.
3R–OH + PX3 → 3R–X + H3PO3
Na podstawie: K.-H. Lautenschläger, W. Schröter, A. Wanninger,
Nowoczesne kompendium chemii, Warszawa 2007.
Napisz wzór elektronowy bromku fosforu(III). Pary elektronowe wiązań oraz wolne pary elektronowe zaznacz kreskami. Oceń, czy cząsteczka bromku fosforu(III) jest płaska.
Wzór:
Ocena: …………………………………………………………………………………………………………………..
Schemat punktowania
1 p. – za poprawne napisanie wzoru elektronowego bromku fosforu(III) i poprawną ocenę.
0 p. – za odpowiedź niepełną lub niepoprawną albo brak odpowiedzi.
Poprawna odpowiedź
Wzór:


Ocena: Cząsteczka nie jest płaska lub ma kształt piramidy trygonalnej lub jest przestrzenna.
Uwaga: Narysowanie wzoru PBr3, w którym elektrony par elektronowych przedstawione są kropkami, należy uznać za poprawne.
