Zadania maturalne z chemii
Zadanie 19. CKE Maj 2019 PR (formuła 2015-2022)
Przeprowadzono doświadczenie, w którym do probówki I wlano kwas solny o pH = 2, a do probówki II – wodny roztwór kwasu octowego (etanowego) o pH = 2. Roztwory miały temperaturę 298 K. Następnie do obu probówek dodano po 1 gramie pyłu cynkowego. Opisane doświadczenie zilustrowano poniższym schematem.


Oceń, czy podane poniżej informacje są prawdziwe. Zaznacz P, jeśli informacja jest prawdziwa, albo F – jeśli jest fałszywa.
| 1. | W warunkach doświadczenia stężenie molowe kwasu solnego jest większe niż stężenie molowe wodnego roztworu kwasu octowego. | P | F |
| 2. | Użycie w doświadczeniu wodnych roztworów o pH = 3 skutkowałoby wzrostem szybkości reakcji wyłącznie w probówce II, ponieważ kwas uczestniczący w tej przemianie jest kwasem słabym. | P | F |
| 3. | Ochłodzenie obu użytych w doświadczeniu wodnych roztworów skutkowałoby zmniejszeniem szybkości wydzielania gazu w przemianach zachodzących w probówkach I i II. | P | F |
Schemat punktowania
1 p. – za poprawne wskazanie trzech odpowiedzi.
0 p. – za odpowiedź niepełną lub niepoprawną albo brak odpowiedzi.
Poprawna odpowiedź
1. – F, 2. – F, 3. – P
Zadanie 7. CKE Maj 2019 PR (formuła 2015-2022)
W reaktorze o stałej pojemności znajdowały się tlenek węgla(II) i para wodna zmieszane w stosunku masowym 1 : 1, a sumaryczna liczba moli tych reagentów była równa 20. Stężeniowa stała równowagi reakcji
CO (g) + H2O (g) ⇄ CO2 (g) + H2 (g)
w warunkach prowadzenia procesu wynosi 1.
Oblicz, ile moli wodoru znajdowało się w reaktorze po osiągnięciu stanu równowagi przez układ.
Schemat punktowania
2 p. – za zastosowanie poprawnej metody, poprawne wykonanie obliczeń oraz podanie liczby moli wodoru.
1 p. – za zastosowanie poprawnej metody, ale
– popełnienie błędów rachunkowych prowadzących do błędnego wyniku liczbowego.
lub
– podanie wyniku z błędną jednostką.
0 p. – za zastosowanie błędnej metody obliczenia albo brak rozwiązania.
Uwagi:
- Należy zwrócić uwagę na zależność wyniku końcowego od przyjętych zaokrągleń wyników pośrednich. Za poprawny należy uznać każdy wynik będący konsekwencją zastosowanej poprawnej metody i poprawnych obliczeń.
- Za rozwiązanie, w którym zdający nie przedstawi toku rozumowania prowadzącego do obliczenia początkowej liczby moli CO i H2O, należy przyznać 0 pkt.
Poprawne rozwiązanie
Kc = [CO2] ⋅ [H2]/ [CO] ⋅ [H2O] = 1
początkowa liczba moli
mH2O : mCO = 1 : 1, stąd nH2O · MH2O = nCO · MCO
nH2O : nCO = 28 : 18
nH2O + nCO = 20 moli
nH2O = 12,2 mola
nCO = 7,8 mola
| liczba moli | początkowa | reakcja | równowaga |
|---|---|---|---|
| CO | 7,8 | –x | 7,8 – x |
| H2O | 12,2 | –x | 12,2 – x |
| H2 | 0 | x | x |
| CO2 | 0 | x | x |
Ponieważ V = const, działania na stężeniach są równoznaczne z działaniami na molach.
Kc = 1, stąd
[CO2][H2] = [CO][H2O]
x2 = (7,8 – x) (12,2 – x)
x2 = 7,8 · 12,2 – 7,8x – 12,2x + x2
x = n = 4,76 (mola) ≈ 4,8 (mola)
Zadanie 6. CKE Maj 2019 PR (formuła 2015-2022)
W przemyśle wodór można otrzymać w procesie konwersji metanu będącego głównym składnikiem gazu ziemnego. W mieszaninie gazu ziemnego i pary wodnej w pewnej temperaturze T i w obecności katalizatora niklowego zachodzą m.in. reakcje opisane poniższymi równaniami.
I CH4 (g) + H2O (g) ⇄ CO (g) + 3H2 (g)
II CH4 (g) + 2H2O (g) ⇄ CO2 (g) + 4H2 (g)
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2004.
Oceń, czy podane poniżej informacje są prawdziwe. Zaznacz P, jeśli informacja jest prawdziwa, albo F – jeśli jest fałszywa.
| 1. | Obniżenie ciśnienia w warunkach izotermicznych (T = const) w reaktorze skutkuje wzrostem wydajności otrzymywania wodoru w reakcjach I i II. | P | F |
| 2. | Wzbogacenie gazu ziemnego metanem skutkuje spadkiem wydajności otrzymywania wodoru w reakcjach I i II. | P | F |
| 3. | Gdy do mieszaniny reakcyjnej w stanie równowagi wprowadzi się katalizator niklowy, to nastąpi wzrost wydajności otrzymywania wodoru w reakcjach I i II. | P | F |
Schemat punktowania
1 p. – za poprawne wskazanie trzech odpowiedzi.
0 p. – za odpowiedź niepełną lub niepoprawną albo brak odpowiedzi.
Poprawna odpowiedź
1. – P, 2. – F, 3. – F
Zadanie 4. CKE Czerwiec 2019 PR (formuła 2015-2022)
Stężeniowa stała równowagi reakcji
CO (g) + H2O (g) ⇄ CO2 (g) + H2 (g)
w temperaturze 1000 K jest równa 1.
Na podstawie: J. Sawicka, A. Janich-Kilian, W. Cejner-Mania, G. Urbańczyk, Tablice chemiczne, Gdańsk 2001.
W reaktorze o stałej pojemności znajdowało się 6 moli tlenku węgla(II).
Oblicz, ile moli wody (w postaci pary wodnej) należy wprowadzić do reaktora, aby po ustaleniu się równowagi w temperaturze 1000 K liczba moli wodoru była dwa razy większa od liczby moli tlenku węgla(II).
Schemat punktowania
2 p. – za zastosowanie poprawnej metody, poprawne wykonanie obliczeń oraz podanie wyniku w molach.
1 p. – zastosowanie poprawnej metody, ale
– popełnienie błędów rachunkowych prowadzących do błędnego wyniku liczbowego
lub
– niepodanie wyniku w molach.
0 p. – za zastosowanie błędnej metody obliczenia albo brak rozwiązania.
Poprawne rozwiązanie
Ponieważ V = const i łączna liczba moli gazowych substratów jest równa łącznej liczbie moli gazowych produktów, w obliczeniach z zastosowaniem stałej równowagi reakcji stężenie molowe można zastąpić liczbą moli reagentów.
| Wzór reagenta | CO | H2O | CO2 | H2 |
| Początkowa liczba moli | 6 | x | 0 | 0 |
| Zmiana liczby moli | – y | – y | + y | + y |
| Liczba moli w stanie równowagi | 6 – y | x – y | y | y |
K = [CO2] ⋅ [H2]/[CO] ⋅ [H2O] ⇒ 1 = y ⋅ y/[(6 − y) ⋅ (x − y)]
i nH2 / nCO = 2 ⇒ y / (6 − y) = 2 ⇒ y = 4 mole ⇒
1 = 4 ⋅ 4 / (6 − 4) ⋅ (x − 4) ⇒ x = 12 (moli)
Zadanie 27. CKE Maj 2020 PR (formuła 2015-2022)
Pewna amina w roztworze wodnym ulega przemianie zgodnie z poniższym równaniem:
Przygotowano wodny roztwór tej aminy w temperaturze 25°C. W otrzymanym roztworze stopień dysocjacji aminy jest równy 3,1%, a pH tego roztworu wynosi 12,2.
27.1.
Oblicz stałą dysocjacji zasadowej Kb tej aminy w temperaturze 25°C, a następnie wybierz i podkreśl jej wzór.
Obliczenia:
Wzór:
27.2.
Rozstrzygnij, czy dodanie stałego wodorotlenku potasu do opisanego roztworu tej aminy będzie miało wpływ na wartość jej stopnia dysocjacji. Uzasadnij swoją odpowiedź.
Rozstrzygnięcie:
……………………………………………………………………………………………………..
Uzasadnienie:
……………………………………………………………………………………………………..
……………………………………………………………………………………………………..
27.1. (0–2)
Zasady oceniania
2 pkt – zastosowanie poprawnej metody, poprawne wykonanie obliczeń, podanie wyniku jako wielkości niemianowanej oraz podkreślenie wzoru półstrukturalnego (grupowego) aminy.
1 pkt – zastosowanie poprawnej metody, ale:
– popełnienie błędów rachunkowych prowadzących do błędnego wyniku.
LUB
– podanie wyniku z niepoprawną jednostką.
LUB
– wskazanie niepoprawnego wzoru aminy lub niepodanie wzoru aminy.
0 pkt – zastosowanie błędnej metody obliczenia albo brak rozwiązania.
Przykładowe rozwiązania
Rozwiązanie I:
pH = 12,2
pOH = 14 – 12,2 = 1,8
pOH = – log[OH−] [OH−] = 0,16·10−1 mol∙dm−3 = cz
K = α2 ∙ c0
K = α2 ∙ czα
K = α ∙ cz
K = 0,000496
K = 5 ∙10−4
Wzór:
Rozwiązanie II:

![]()
Wzór:
27.2. (0–1)
Zasady oceniania
1 pkt – poprawne rozstrzygnięcie i poprawne uzasadnienie odwołujące się do mechanizmu procesu równowagowego zachodzącego w roztworze.
0 pkt – odpowiedź niepełna lub niepoprawna albo brak odpowiedzi.
Poprawna odpowiedź
Rozstrzygnięcie: Tak, (będzie miało wpływ na wartość stopnia dysocjacji.)
Uzasadnienie: (Nastąpi zmniejszenie stopnia dysocjacji, ponieważ) wzrost stężenia jonów OH− poskutkuje zgodnie z regułą przekory:
– zmniejszeniem wydajności przemiany.
ALBO
– przesunięciem równowagi w lewo.
ALBO
– przesunięciem równowagi w kierunku substratów.
Zadanie 12. CKE Maj 2020 PR (formuła 2015-2022)
Do zbiornika, z którego wypompowano powietrze, wprowadzono tlenek azotu(IV) o wzorze NO2 i po zamknięciu utrzymywano temperaturę 25°C do momentu osiągnięcia przez układ stanu równowagi opisanej poniższym równaniem:
Zmiany stężenia obu reagentów przedstawiono na poniższym wykresie.

Na podstawie: J. McMurry, R. Fay, Chemistry, Upper Saddle River 2001.
Oblicz stężeniową stałą równowagi opisanej reakcji w temperaturze 25 °C oraz uzupełnij zdanie – wybierz i podkreśl jedną odpowiedź spośród podanych w nawiasie.
Obliczenia:
Stężeniowa stała równowagi opisanej reakcji w temperaturze wyższej niż 25°C jest (mniejsza niż / większa niż / taka sama jak) stężeniowa stała równowagi tej reakcji w temperaturze 25°C.
Zasady oceniania
2 pkt – poprawne obliczenie i podanie wyniku jako wielkości niemianowanej oraz poprawne uzupełnienie zdania.
1 pkt – poprawne obliczenie i podanie wyniku jako wielkości niemianowanej oraz błędne uzupełnienie zdania albo brak uzupełnienia zdania.
LUB
– błędne obliczenie lub podanie wyniku z błędną jednostką albo brak obliczenia oraz poprawne uzupełnienie zdania.
0 p. – odpowiedź niespełniająca powyższych kryteriów albo brak rozwiązania
Przykładowe rozwiązanie
Stała równowagi reakcji w t = 25 °C: K = [N2O4] / [NO2]2 = 0,0337 / (0,0125)2 = 0,0337 / 1,5625 ⋅ 10−4 ≈ 216
Uwaga: Podanie wartości stałej równowagi z jednostką dm3·mol−1 – wynikającą z podstawienia do wyrażenia na K stężenia molowego reagentów – nie skutkuje utratą punktu.
Stężeniowa stała równowagi opisanej reakcji w temperaturze wyższej niż 25°C jest (mniejsza niż / większa niż / taka sama jak) stężeniowa stała równowagi tej reakcji w temperaturze 25°C.
Zadanie 7. CKE Maj 2015 PR (formuła 2015-2022)
Poniżej przedstawiono model struktury wody w stanie stałym.
Uzupełnij zdania opisujące budowę i właściwości lodu. Podkreśl właściwe określenie spośród wymienionych w każdym nawiasie.
W wodzie w stanie stałym, czyli w lodzie, każda cząsteczka wody związana jest wiązaniami (kowalencyjnymi / kowalencyjnymi spolaryzowanymi / wodorowymi / jonowymi) z czterema innymi cząsteczkami wody leżącymi w narożach czworościanu foremnego. Tworzy się w ten sposób luźna sieć cząsteczkowa o strukturze (diagonalnej / trygonalnej / tetraedrycznej), która pęka, gdy lód się topi, choć pozostają po niej skupiska zawierające 30 i więcej cząsteczek. W ciekłej wodzie cząsteczki zajmują przestrzeń mniejszą niż w sieci krystalicznej, a zatem woda o temperaturze zamarzania ma gęstość (większą / mniejszą) niż lód. Dlatego lód (tonie w / pływa po) wodzie.
Na podstawie: K.-H. Lautenschläger, W. Schröter, A. Wanninger, Nowoczesne kompendium chemii, Warszawa 2007.
Schemat punktowania
1 p. – za poprawne wskazanie określeń w każdym nawiasie.
0 p. – za odpowiedź niepełną lub błędną albo brak odpowiedzi.
Poprawna odpowiedź
W wodzie w stanie stałym, czyli w lodzie, każda cząsteczka wody związana jest wiązaniami (kowalencyjnymi / kowalencyjnymi spolaryzowanymi / wodorowymi / jonowymi) z czterema innymi cząsteczkami wody leżącymi w narożach czworościanu foremnego. Tworzy się w ten sposób luźna sieć cząsteczkowa o strukturze (diagonalnej / trygonalnej / tetraedrycznej), która pęka, gdy lód się topi, choć pozostają po niej skupiska zawierające 30 i więcej cząsteczek. W ciekłej wodzie cząsteczki zajmują przestrzeń mniejszą niż w sieci krystalicznej, a zatem woda o temperaturze zamarzania ma gęstość (większą / mniejszą) niż lód. Dlatego lód (tonie w / pływa po) wodzie.
Zadanie 5. CKE Maj 2015 PR (formuła 2015-2022)
Budowa cząsteczki tlenku siarki(VI) jest skomplikowana. Poniżej przedstawiono jeden ze wzorów opisujących strukturę elektronową SO3.
5.1.
Określ typ hybrydyzacji orbitali atomu siarki (sp, sp2, sp3) i geometrię cząsteczki (liniowa, płaska, tetraedryczna).
Typ hybrydyzacji: ………………………………….
Geometria: ………………………………….
5.2.
Napisz, ile wiązań σ i π występuje w cząsteczce SO3 o przedstawionej powyżej strukturze.
Liczba wiązań σ: ………………………………….
Liczba wiązań π: ………………………………….
5.1. (0–1)
Schemat punktowania
1 p. – za poprawne określenie hybrydyzacji i geometrii cząsteczki.
0 p. – za odpowiedź niepełną lub błędną albo brak odpowiedzi.
Poprawna odpowiedź
Typ hybrydyzacji: sp2
Geometria: płaska
5.2. (0–1)
Schemat punktowania
1 p. – za poprawne określenie liczby wiązań σ i π.
0 p. – za odpowiedź niepełną lub błędną albo brak odpowiedzi.
Poprawna odpowiedź
Liczba wiązań σ: 3
Liczba wiązań π: 1
Zadanie 4. CKE Maj 2015 PR (formuła 2015-2022)
Brom występuje w przyrodzie w postaci mieszaniny dwóch izotopów o masach atomowych równych 78,92 u i 80,92 u. Średnia masa atomowa bromu jest równa 79,90 u. Pierwiastek ten w reakcjach utleniania i redukcji może pełnić funkcję zarówno utleniacza, jak i reduktora. Tworzy związki chemiczne, w których występują różne rodzaje wiązań.
Ustal i wpisz do tabeli, jaki rodzaj wiązania (kowalencyjne niespolaryzowane, kowalencyjne spolaryzowane, jonowe) występuje w wymienionych związkach.
| CBr4 | CaBr2 | HBr | |
|---|---|---|---|
| Rodzaj wiązania |
Schemat punktowania
1 p. – za poprawne uzupełnienie całej tabeli.
0 p. – za odpowiedź niepełną lub błędną albo brak odpowiedzi.
Poprawna odpowiedź
| CBr4 | CaBr2 | HBr | |
|---|---|---|---|
| Rodzaj wiązania | kowalencyjne (niespolaryzowane) lub kowalencyjne spolaryzowane | jonowe | kowalencyjne spolaryzowane |
Zadanie 33. CKE Maj 2016 PR (formuła 2015-2022)
W cząsteczce kwasu askorbinowego (witaminy C) występują dwa enolowe atomy węgla, czyli atomy węgla o hybrydyzacji sp2 z przyłączonymi grupami hydroksylowymi. Cząsteczka tego związku zawiera ponadto dwa asymetryczne atomy węgla – o hybrydyzacji sp3 z przyłączonymi czterema różnymi podstawnikami. Poniżej przedstawiono wzór witaminy C, w którym małymi literami oznaczono poszczególne atomy węgla.
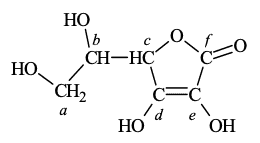
Napisz litery (a–f), którymi oznaczono w powyższym wzorze kwasu askorbinowego wszystkie enolowe atomy węgla oraz wszystkie asymetryczne atomy węgla.
Schemat punktowania
1 p. – za poprawny wybór dwóch enolowych atomów węgla i dwóch asymetrycznych atomów węgla.
0 p. – za odpowiedź niepełną lub błędną albo brak odpowiedzi.
Poprawna odpowiedź
Enolowe atomy węgla: d, e
Asymetryczne atomy węgla: b, c
