Gaz syntezowy, czyli mieszanina CO i H2, jest otrzymywany w przemyśle różnymi metodami. Niżej podano równania dwóch reakcji, w których powstaje taka mieszanina.
I CH4 + CO2 → 2CO + 2H2 ΔH<0
II CH4 + H2O → CO + 3H2 ΔH>0
Na poniższym wykresie przedstawiono zależność stopnia przemiany metanu od temperatury dla dwóch różnych wartości ciśnienia dla jednej z tych reakcji. Stopień przemiany metanu jest miarą wydajności reakcji – im większy stopień przemiany, tym większa wydajność reakcji.
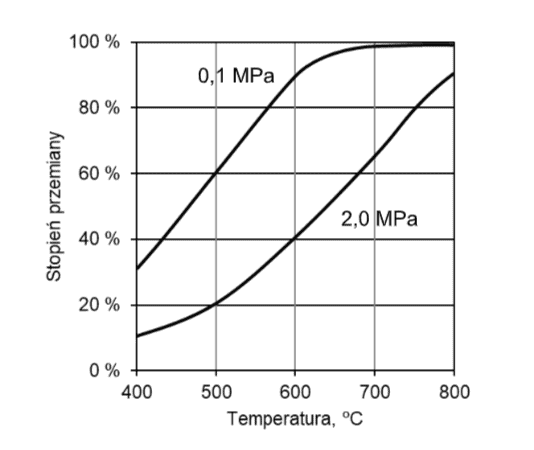
Na podstawie: M. Pańczyk, T. Borowiecki, Otrzymywanie i zastosowanie gazu syntezowego, Lublin 2013.
a) Napisz numer reakcji (I albo II), do której odnosi się powyższy wykres stopnia przemiany metanu. Odpowiedź uzasadnij – uwzględnij efekt energetyczny reakcji.
Numer reakcji: ………………………
Uzasadnienie:
………………………………………………………………………………………………………………………………………………
………………………………………………………………………………………………………………………………………………
b) Uzupełnij zdanie o wpływie ciśnienia na stopień przemiany metanu – wybierz i zaznacz jedną odpowiedź spośród podanych w nawiasie. Wyjaśnij przedstawioną na wykresie zależność stopnia przemiany metanu od ciśnienia.
W stałej temperaturze wzrost ciśnienia skutkuje (wzrostem / spadkiem) stopnia przemiany metanu.
Wyjaśnienie:
………………………………………………………………………………………………………………………………………………
………………………………………………………………………………………………………………………………………………

Responses