Zadania maturalne z chemii
Zadanie 21. CKE Czerwiec 2019 PR (formuła 2015-2022)
Do probówek, zawierających przygotowany wcześniej odczynnik, wprowadzono dwa różne związki: do probówki I – propan-2-ol, a do probówki II – propano-1,2-diol. Zawartość każdej probówki wymieszano. Objawy reakcji zaobserwowano tylko w jednej probówce.
21.1. (0−1)
Uzupełnij schemat doświadczenia. Wybierz i podkreśl nazwę użytego odczynnika.
Odczynnik:
- świeżo wytrącony wodorotlenek miedzi(II)
- zakwaszony roztwór manganianu(VII) potasu
- woda bromowa z dodatkiem wodorowęglanu sodu
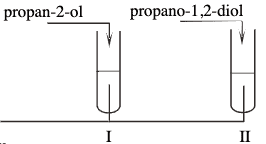
21.2. (0−1)
Opisz zmiany możliwe do zaobserwowania po dodaniu propan-2-olu i propano-1,2-diolu do wybranego odczynnika. Uwzględnij wygląd zawartości probówek przed reakcją i po dodaniu badanych związków.
| Wygląd zawartości probówki | ||
| przed reakcją | po reakcji | |
| Probówka I | ||
| Probówka II | ||
21.1. (0–1)
Schemat punktowania
1 p. – za uzupełnienie schematu doświadczenia – poprawny wybór i zaznaczenie odczynnika.
0 p. – za odpowiedź niepoprawną albo brak odpowiedzi.
Poprawna odpowiedź
- świeżo wytrącony wodorotlenek miedzi(II)
21.2. (0–1)
Schemat punktowania
1 p. – za poprawny opis zmian przy poprawnym wyborze i zaznaczeniu odczynnika
w zadaniu 21.1.
0 p. – za błędny opis zmian lub błędny wybór, lub brak zaznaczenia odczynnika w zadaniu 21.1 albo brak odpowiedzi.
Poprawna odpowiedź
| Wygląd zawartości probówki | ||
| przed reakcją | po reakcji | |
| Probówka I | niebieski osad | (niebieski) osad nie ulega zmianie lub brak objawów reakcji |
| Probówka II | (niebieski) osad roztwarza się lub powstaje szafirowy roztwór | |
Zadanie 31. CKE Maj 2020 PR (formuła 2015-2022)
Serotonina, nazywana hormonem szczęścia, powstaje z aminokwasu białkowego – tryptofanu. W pierwszym etapie przedstawionego poniżej ciągu przemian tryptofan ulega reakcji substytucji, w wyniku czego powstaje hydroksylowa pochodna, która następnie przekształca się w serotoninę. W kolejnych przemianach z serotoniny powstaje melatonina.
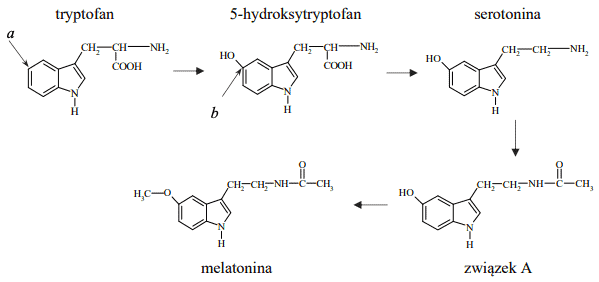
W dwóch nieoznakowanych probówkach znajdują się serotonina i melatonina.
Uzupełnij poniższe zdanie dotyczące możliwości rozróżnienia tych związków. Wybierz i podkreśl jedną odpowiedź spośród podanych w każdym nawiasie.
Zawartość obu probówek (może / nie może) być rozróżniona za pomocą wodnego roztworu chlorku żelaza(III), ponieważ (tylko w cząsteczkach melatoniny / tylko w cząsteczkach serotoniny / w cząsteczkach obu związków) występuje (ugrupowanie fenolowe / wiązanie amidowe / wiązanie estrowe).
Zasady oceniania
1 pkt – poprawne uzupełnienie zdania.
0 pkt – odpowiedź niepełna lub niepoprawna albo brak odpowiedzi.
Poprawna odpowiedź
Zawartość obu probówek (może / nie może) być rozróżniona za pomocą wodnego roztworu chlorku żelaza(III), ponieważ (tylko w cząsteczkach melatoniny / tylko w cząsteczkach serotoniny / w cząsteczkach obu związków) występuje (ugrupowanie fenolowe / wiązanie amidowe / wiązanie estrowe).
Zadanie 36. CKE Maj 2015 PR (formuła 2015-2022)
Liczba jodowa jest miarą liczby wiązań nienasyconych, np. w tłuszczach. Określa ona liczbę gramów jodu, który może przyłączyć w warunkach standardowych 100 gramów tłuszczu.
Na podstawie: Encyklopedia szkolna. Chemia, Kraków 2005.
Poniżej podano wzory trzech tłuszczów.
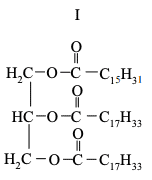
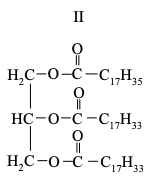
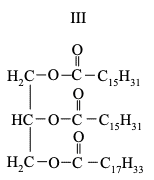
Uszereguj tłuszcze o podanych wzorach zgodnie ze wzrastającą liczbą jodową − zapisz w kolejności numery, którymi je oznaczono.
……………………………………………………………………………………………………..
Schemat punktowania
1 p. – za poprawne uszeregowanie wzorów trzech tłuszczów.
0 p. – za błędną odpowiedź albo brak odpowiedzi.
Poprawna odpowiedź
III, II, I
Zadanie 32. CKE Maj 2016 PR (formuła 2015-2022)
Kwas 2-hydroksypropanowy w reakcji ze związkiem X tworzy ester o wzorze sumarycznym C5H8O4. Orbitalom walencyjnym każdego z atomów węgla budujących cząsteczkę związku X przypisuje się inny typ hybrydyzacji. Ponadto wiadomo, że w cząsteczce związku X występuje tylko jedna grupa funkcyjna.
Ustal wzór związku X, którego użyto do estryfikacji kwasu 2-hydroksypropanowego, i napisz równanie reakcji otrzymywania opisanego estru. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.
Schemat punktowania
1 p. – za poprawne napisanie równania reakcji.
0 p. – za napisanie błędnego równania reakcji (błędne wzory, błędne współczynniki stechiometryczne) albo brak odpowiedzi.
Poprawna odpowiedź
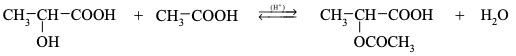
Zadanie 34. CKE Maj 2017 PR (formuła 2015-2022)
Poniżej przedstawiono wzór kwasu winowego:
HOOC–CH(OH)–CH(OH)–COOH
Napisz wzór półstrukturalny (grupowy) organicznego produktu reakcji kwasu winowego z metanolem użytym w nadmiarze w środowisku stężonego kwasu siarkowego(VI).
…………………………………………………………………………………………………………………………
Schemat punktowania
1 p. – za poprawne napisanie produktu reakcji.
0 p. – za odpowiedź błędną albo brak odpowiedzi.
Poprawna odpowiedź
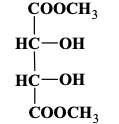
Zadanie 25. CKE Maj 2019 PR (formuła 2015-2022)
Detergenty są składnikami powszechnie używanych środków czyszczących i piorących. Wśród stosowanych obecnie detergentów można wyróżnić detergenty kationowe i anionowe. Przykładem detergentu anionowego jest związek o wzorze
CH3‒(CH2)10‒CH2‒OSO3− Na+
Można go otrzymać w reakcji estryfikacji z udziałem alkoholu o długim prostym łańcuchu węglowym i odpowiedniego kwasu. Tak uzyskany ester poddaje się reakcji z wodorotlenkiem sodu, w wyniku czego otrzymuje się środek powierzchniowo czynny, który – podobnie jak mydła – zawiera dwa fragmenty: niepolarny i polarny.
Podaj wzory sumaryczne alkoholu i kwasu nieorganicznego, których należy użyć w opisanym procesie otrzymania tego detergentu.
Wzór sumaryczny alkoholu: ………………………………………………….
Wzór sumaryczny kwasu nieorganicznego: ………………………………………………….
Schemat punktowania
1 p. – za poprawne podanie wzoru alkoholu i wzoru kwasu.
0 p. – za odpowiedź niepełną lub niepoprawną albo brak odpowiedzi.
Poprawna odpowiedź
Wzór sumaryczny alkoholu: C12H26O lub C12H25OH
Uwaga: Podanie wzoru CH3‒(CH2)10‒CH2‒OH należy uznać za poprawne.
Wzór sumaryczny kwasu nieorganicznego: H2SO4
Zadanie 17. CKE Maj 2015 PR (formuła 2015-2022)
Pewien proces, w którym związek A zostaje przekształcony w związek B, przebiega w dwóch etapach.
| Etap 1. | A → C | ΔH < 0 |
| Etap 2. | C → B | ΔH > 0 |
Przeanalizuj poniższe wykresy i ustal, który z nich odpowiada opisanej przemianie.
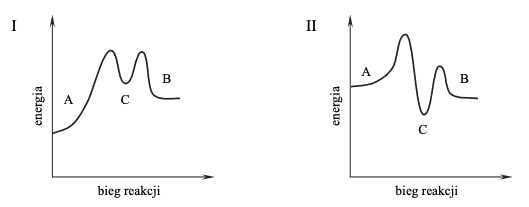
Opisaną przemianę poprawnie zilustrowano na wykresie ……….. .
Schemat punktowania
1 p. – za wskazanie właściwego wykresu.
0 p. – za błędną odpowiedź albo brak odpowiedzi.
Poprawna odpowiedź
Opisaną przemianę poprawnie zilustrowano na wykresie II.
Zadanie 5. CKE Maj 2016 PR (formuła 2015-2022)
W wyniku pewnej odwracalnej reakcji chemicznej z dwóch substratów powstaje jeden produkt. Przemiana przebiega w fazie gazowej, co oznacza, że oba substraty i produkt są gazami. Reakcję tę przeprowadzono w zamkniętym reaktorze przy użyciu stechiometrycznych ilości substratów w różnych temperaturach i pod różnym ciśnieniem. Na poniższym diagramie przedstawiono, jaki procent objętości mieszaniny poreakcyjnej w reaktorze stanowiła objętość produktu tej reakcji w zależności od warunków temperatury i ciśnienia, w jakich przebiegała.
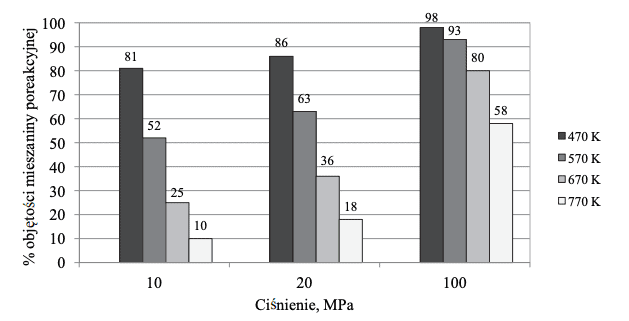
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2010.
Na podstawie analizy diagramu określ, czy w czasie opisanej reakcji układ oddaje energię do otoczenia, czy przyjmuje ją od otoczenia. Odpowiedź uzasadnij.
……………………………………………………………………………………………………..
Schemat punktowania
1 p. – za poprawną odpowiedź i poprawne uzasadnienie.
0 p. – za odpowiedź niepełną lub błędną albo brak odpowiedzi.
Przykłady poprawnej odpowiedzi
- Wnioskujemy, że w czasie reakcji układ oddaje energię do otoczenia, ponieważ zgodnie z regułą przekory wydajność reakcji maleje ze wzrostem temperatury.
- Reakcja jest egzoenergetyczna (lub egzotermiczna), ponieważ zgodnie z regułą przekory wydajność reakcji maleje ze wzrostem temperatury.
- Wnioskujemy, że w czasie reakcji układ oddaje energię do otoczenia, ponieważ wraz ze wzrostem temperatury maleje procent objętości produktu w mieszaninie.
Zadanie 24. CKE Maj 2017 PR (formuła 2015-2022)
W wysokiej temperaturze może zachodzić rozkład metanu na substancje proste zgodnie z równaniem:
CH4 (g) ⇄ C (s) + 2H2 (g)
Miarą wydajności tej reakcji jest równowagowy stopień przemiany metanu x, który wyraża się wzorem:
x = n0[CH4] − n[CH4]n0[CH4]
W tym wzorze n0[CH4] oznacza początkową liczbę moli metanu, a n[CH4] – liczbę moli tego gazu pozostałego po ustaleniu się stanu równowagi. Poniżej przedstawiono zależność równowagowego stopnia przemiany metanu x od temperatury dla trzech wartości ciśnienia.
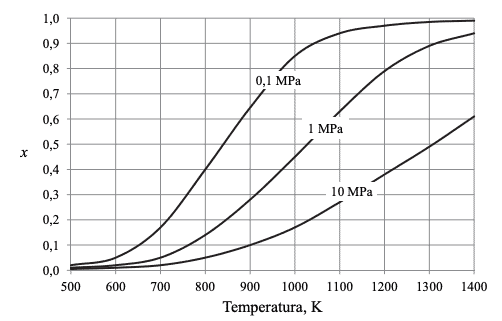
Na podstawie: P. Schmidt-Szałowski, M. Szafran, E. Bobryk, J. Sentek,
Technologia chemiczna. Przemysł nieorganiczny, Warszawa 2013.
Określ, czy ΔH opisanej reakcji rozkładu metanu jest większa od zera, czy – mniejsza od zera. Odpowiedź uzasadnij.
……………………………………………………………………………………………………..
……………………………………………………………………………………………………..
Schemat punktowania
1 p. – za poprawne określenie, czy dla opisanej reakcji ΔH < 0, czy ΔH > 0 i poprawne uzasadnienie odwołujące się do stopnia przemiany metanu lub wydajności procesu.
0 p. – za inną odpowiedź lub brak odpowiedzi.
Przykłady poprawnej odpowiedzi
- Dla reakcji rozkładu metanu ΔH > 0, ponieważ wydajność tej reakcji wzrasta ze wzrostem temperatury.
- ΔH tej reakcji jest większa od zera, ponieważ im wyższa jest temperatura, tym równowagowy stopień przemiany jest większy.
Zadanie 5. CKE Maj 2018 PR (formuła 2015-2022)
W wysokiej temperaturze węgiel reaguje z tlenkiem węgla(IV) i ustala się równowaga chemiczna:
CO2 (g) + C (s) ⇄ 2CO (g)
Objętościową zawartość procentową CO i CO2 w gazie pozostającym w równowadze z węglem w zależności od temperatury (pod ciśnieniem atmosferycznym 1013 hPa) przedstawiono na poniższym wykresie.
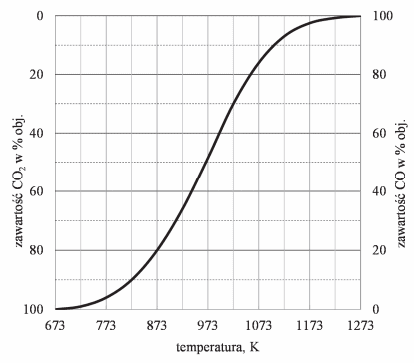
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2004.
Oceń, czy reakcja pomiędzy tlenkiem węgla(IV) i węglem jest procesem endo- czy egzoenergetycznym. Odpowiedź uzasadnij.
……………………………………………………………………………………………………..
……………………………………………………………………………………………………..
Schemat punktowania
1 p. – za poprawne wskazanie, czy opisana przemiana jest procesem egzoenergetycznym, czy endoenergetycznym, wraz z uzasadnieniem, które odwołuje się do kierunku zmiany wydajności reakcji pod wpływem zmiany temperatury.
0 p. – za odpowiedź niepełną lub błędną albo brak odpowiedzi.
Przykłady poprawnej odpowiedzi
Przemiana jest procesem endoenergetycznym. Wraz ze wzrostem temperatury wzrasta zawartość (a więc stężenie) CO, czyli zwiększa się wydajność reakcji.
lub
Przemiana jest procesem endoenergetycznym. Wraz ze wzrostem temperatury wzrasta procent objętościowy CO.
lub
Przemiana jest procesem endoenergetycznym, ponieważ im wyższa temperatura tym więcej CO w mieszaninie równowagowej.
Uwaga! Stwierdzenie: ∆H > 0 nie jest uzasadnieniem.
Uwaga! Za uzasadnienie zawierające stwierdzenie, że wraz ze wzrostem temperatury wzrasta objętość CO, należy przyznać 0 punktów.
