Zadania maturalne z chemii
Zadanie 22. CKE Maj 2019 PP (formuła do 2015)
Danych jest pięć par związków.
- CH3–CH2–CO‒CH3 i CH3‒CH(CH3)‒CHO
- CH3–CH2–CH2–CHBr–CH3 i CH3–CHBr–CH2–CH3
- HCOOH i CH3COOH
- CH2=CH–CH=CH2 i CH3–C≡C–CH3
- CH2(OH)–CH2 (OH) i CH2(OH)–CH2–CH3
Podaj nazwy systematyczne związków stanowiących parę oznaczoną numerem 1.
……………………………………………………………………………………………………..
Schemat punktowania
1 p. – za podanie poprawnych nazw systematycznych dwóch związków.
0 p. – za odpowiedź niepełną lub niepoprawną albo brak odpowiedzi.
Poprawna odpowiedź
butanon, 2-metylopropanal
Zadanie 39. CKE Maj 2015 PR (formuła 2015-2022)
W czterech naczyniach (I–IV) znajdowały się wodne roztwory: glukozy, fenolu (benzenolu), glicerolu (propano-1,2,3-triolu) i glicyloalanyloglicyny. W celu ich identyfikacji przeprowadzono trzy serie doświadczeń. W pierwszej serii doświadczeń, po dodaniu wodnego roztworu chlorku żelaza(III) do próbek pobranych z czterech naczyń, próbka z naczynia I przyjęła fioletowe zabarwienie. W drugiej serii doświadczeń, po dodaniu świeżo strąconego wodorotlenku miedzi(II) do próbek pobranych z trzech naczyń (II, III i IV), próbka z naczynia II przyjęła fioletowe zabarwienie, a w pozostałych próbkach pojawiło się szafirowe zabarwienie. W trzeciej serii doświadczeń, po ogrzaniu szafirowych roztworów otrzymanych w serii drugiej, w roztworze powstałym z próbki z naczynia III pojawił się ceglasty osad.
Napisz, jaki element budowy cząsteczek związków znajdujących się w roztworach z naczyń III i IV zadecydował o powstaniu szafirowego zabarwienia roztworów w drugiej serii doświadczeń.
……………………………………………………………………………………………………..
Schemat punktowania
1 p. – za poprawne wskazanie elementu budowy glicerolu i glukozy.
0 p. – za błędną odpowiedź albo brak odpowiedzi.
Poprawna odpowiedź
Obecność grup hydroksylowych – wicynalnych lub położonych przy sąsiednich atomach węgla – w cząsteczkach glicerolu i glukozy.
Zadanie 28. CKE Maj 2015 PR (formuła 2015-2022)
W cząsteczce pewnego optycznie czynnego nasyconego łańcuchowego alkoholu monohydroksylowego o nierozgałęzionym łańcuchu jest pięć atomów węgla. W wyniku utlenienia tego alkoholu powstaje keton.
Narysuj wzór półstrukturalny (grupowy), podaj nazwę systematyczną oraz określ rzędowość opisanego alkoholu.
Wzór: ……………………………….
Nazwa: ……………………………….
Rzędowość: ……………………………….
Schemat punktowania
2 p. – za poprawne napisanie wzoru i nazwy alkoholu oraz poprawne określenie jego
rzędowości.
1 p. – za poprawne napisanie wzoru alkoholu i podanie błędnej nazwy lub błędne określenie jego rzędowości.
0 p. – za odpowiedź niepełną lub błędną albo brak odpowiedzi.
Poprawna odpowiedź
Wzór: CH3 – CH(OH) – CH2 – CH2 – CH3
Nazwa: pentan-2-ol
Rzędowość: II-rzędowy
Zadanie 25. CKE Maj 2016 PR (formuła 2015-2022)
Woda przyłącza się do alkenów w obecności silnie kwasowego katalizatora H3O+ . Addycja ta przebiega poprzez tworzenie kationów z ładunkiem dodatnim zlokalizowanym na atomie węgla, czyli tzw. karbokationów. Mechanizm tej reakcji dla alkenów o wzorze ogólnym R–CH=CH2 (R – grupa alkilowa) można przedstawić w trzech etapach.
Uwaga: w poniższych równaniach etapów reakcji wzór wody przedstawiono jako :OH2, a wzór kwasowego katalizatora zapisano jako H:OH2+.
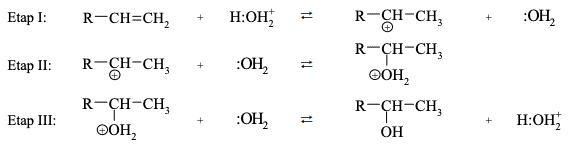
Na podstawie: R. Morrison, R. Boyd, Chemia organiczna, Warszawa 1985.
25.1.
Uzupełnij poniższe zdania. Wybierz i zaznacz jedno właściwe określenie spośród podanych w każdym nawiasie.
Podczas etapu I alken ulega działaniu reagenta (wolnorodnikowego / nukleofilowego / elektrofilowego). W etapie II karbokation łączy się z cząsteczką wody, w wyniku czego powstaje protonowany alkohol. Na tym etapie przemiany woda działa jako (nukleofil / elektrofil). Podczas etapu III protonowany alkohol (oddaje / pobiera) proton, co prowadzi do powstania obojętnego alkoholu oraz do odtworzenia katalizatora.
25.2.
Spośród alkoholi o podanych niżej wzorach wybierz te, których nie można (jako produktu głównego) otrzymać podczas hydratacji alkenów prowadzonej w obecności kwasu. Podkreśl wzory wybranych alkoholi i uzasadnij swój wybór.
Uzasadnienie:
……………………………………………………………………………………………………..
……………………………………………………………………………………………………..
……………………………………………………………………………………………………..
25.1. (0–1)
Schemat punktowania
1 p. – za poprawne wskazanie określeń w każdym nawiasie.
0 p. – za odpowiedź niepełną lub błędną albo brak odpowiedzi.
Poprawna odpowiedź
Podczas etapu I alken ulega działaniu reagenta (wolnorodnikowego / nukleofilowego / elektrofilowego). W etapie II karbokation łączy się z cząsteczką wody, w wyniku czego powstaje protonowany alkohol. Na tym etapie przemiany woda działa jako (nukleofil / elektrofil). Podczas etapu III protonowany alkohol (oddaje / pobiera) proton, co prowadzi do powstania obojętnego alkoholu oraz do odtworzenia katalizatora.
25.2. (0–1)
Schemat punktowania
1 p. – za poprawny wybór wzorów i poprawne uzasadnienie.
0 p. – za odpowiedź niepełną lub błędną albo brak odpowiedzi.
Poprawna odpowiedź
Uzasadnienie: Hydratacja niesymetrycznych alkenów w środowisku kwasowym przebiega zgodnie z regułą Markownikowa.
Uwaga: Poprawne jest uzasadnienie, w którym zdający odwołał się do trwałości karbokationów.
Zadanie 35. CKE Maj 2017 PR (formuła 2015-2022)
Wykonano doświadczenie, w którym do dwóch probówek z tym samym odczynnikiem wprowadzono wodne roztwory dwóch związków chemicznych. Do probówki I wprowadzono wodny roztwór winianu disodu (NaOOC–CH(OH)–CH(OH)–COONa), a do probówki II – wodny roztwór etanianu (octanu) sodu (CH3COONa). W warunkach doświadczenia obydwa wodne roztwory były bezbarwnymi cieczami.
Zaprojektuj doświadczenie, którego przebieg pozwoli na potwierdzenie, że roztwór winianu disodu wprowadzono do probówki I, a roztwór octanu sodu – do probówki II.
35.1.
Uzupełnij schemat doświadczenia. Podkreśl nazwę odczynnika, który – po dodaniu do niego roztworów opisanych związków i wymieszaniu zawartości probówek – umożliwi zaobserwowanie różnic w przebiegu doświadczenia z udziałem winianu disodu i octanu sodu.

35.2.
Opisz zmiany możliwe do zaobserwowania w czasie doświadczenia, pozwalające na potwierdzenie, że do probówki I wprowadzono roztwór winianu disodu, a do probówki II – roztwór octanu sodu.
Probówka I:
…………………………………………………………………………………………………………………………
Probówka II:
…………………………………………………………………………………………………………………………
35.1. (0–1)
Schemat punktowania
1 p. – za poprawny wybór odczynnika i uzupełnienie schematu.
0 p. – za odpowiedź błędną albo brak odpowiedzi.
Poprawna odpowiedź

35.2. (0–1)
Schemat punktowania
1 p. – za poprawny opis zmian przy poprawnym wyborze odczynnika w zadaniu 35.1.
0 p. – za błędny wybór odczynnika w zadaniu 35.1. lub błędny opis zmian albo brak odpowiedzi.
Przykłady poprawnej odpowiedzi
Probówka I: (Niebieski) osad roztworzył się.
lub Powstał (szafirowy) roztwór.
lub Pojawiło się szafirowe zabarwienie.
Probówka II: Brak zmian zawartości probówki.
Zadanie 28. CKE Maj 2017 PR (formuła 2015-2022)
Oznaczanie zawartości fenolu w ściekach przemysłowych możne przebiegać w kilku etapach opisanych poniżej.
Etap I: Otrzymywanie bromu.
Etap II: Bromowanie fenolu.
Etap III: Wydzielanie jodu.
Etap IV: Miareczkowanie jodu.
Gdy do zakwaszonego roztworu fenolu zawierającego nadmiar jonów bromkowych wprowadzi się bromian(V) potasu w nadmiarze w stosunku do fenolu, to wytworzony brom (w ilości równoważnej do bromianu(V) potasu) reaguje z fenolem zgodnie z równaniem (etap II):
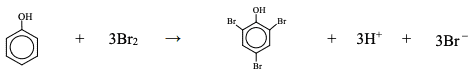
Następnie do powstałej mieszaniny dodaje się jodek potasu. Brom, który nie został zużyty w reakcji bromowania, powoduje wydzielenie równoważnej ilości jodu (etap III):
2I– + Br2 → 2Br– + I2
Podczas kolejnego etapu (etapu IV) jod miareczkuje się wodnym roztworem tiosiarczanu sodu (Na2S2O3), co można zilustrować równaniem:
2S2O32- + I2 → S4O62- + 2I–
Na podstawie: J. Minczewski, Z. Marczenko,
Chemia analityczna – Podstawy teoretyczne i analiza jakościowa, Warszawa 2012.
Uzupełnij poniższe zdania. Wybierz i zaznacz jedno określenie spośród podanych w każdym nawiasie.
Fenol, który jest pochodną benzenu zawierającą grupę hydroksylową związaną z pierścieniem, ulega podczas etapu II oznaczania reakcji substytucji (elektrofilowej / nukleofilowej / rodnikowej). Bromowanie benzenu wymaga użycia katalizatora, natomiast reakcja fenolu z bromem przebiega łatwo już w temperaturze pokojowej. Można więc wnioskować, że grupa hydroksylowa związana z pierścieniem benzenowym (ułatwia / utrudnia) podstawienie atomów (bromu / wodoru) atomami (bromu / wodoru).
Schemat punktowania
1 p. – za poprawne wskazanie określeń w każdym nawiasie.
0 p. – za odpowiedź niepełną lub błędną albo brak odpowiedzi.
Poprawna odpowiedź
Fenol, który jest pochodną benzenu zawierającą grupę hydroksylową związaną z pierścieniem, ulega podczas etapu II oznaczania reakcji substytucji (elektrofilowej / nukleofilowej / rodnikowej). Bromowanie benzenu wymaga użycia katalizatora, natomiast reakcja fenolu z bromem przebiega łatwo już w temperaturze pokojowej. Można więc wnioskować, że grupa hydroksylowa związana z pierścieniem benzenowym (ułatwia / utrudnia) podstawienie atomów (bromu / wodoru) atomami (bromu / wodoru).
Zadanie 32. CKE Maj 2018 PR (formuła 2015-2022)
Poniżej przedstawiono wzory związków oznaczonych numerami 1–5.
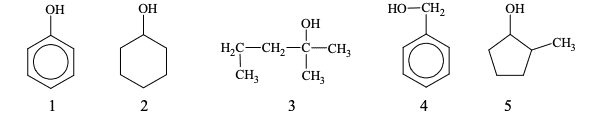
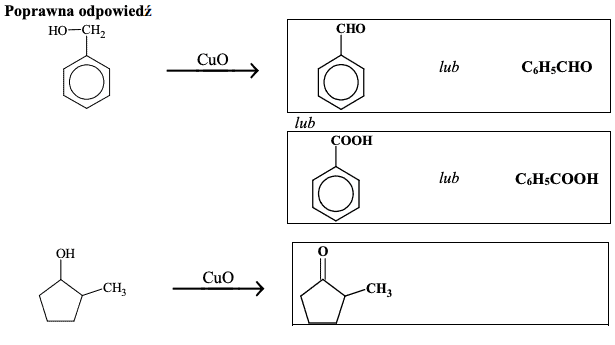
Uzupełnij poniższe schematy. Napisz wzór półstrukturalny (grupowy) lub uproszczony organicznego produktu reakcji tlenku miedzi(II):
- ze związkiem oznaczonym numerem 4.

- ze związkiem oznaczonym numerem 5.

Schemat punktowania
1 p. – za poprawnie napisanie wzorów organicznych produktów reakcji.
0 p. – za odpowiedź niepełną lub błędną albo brak odpowiedzi.
Zadanie 23. CKE Czerwiec 2019 PR (formuła 2015-2022)
Do probówek, zawierających przygotowany wcześniej odczynnik, wprowadzono dwa różne związki: do probówki I – propan-2-ol, a do probówki II – propano-1,2-diol. Zawartość każdej probówki wymieszano. Objawy reakcji zaobserwowano tylko w jednej probówce.
Uzupełnij zdanie. Wybierz i zaznacz odpowiedź A. albo B. oraz jej uzasadnienie 1. albo 2.
Gdyby zamiast propano-1,2-diolu do probówki II wprowadzono 1,4-dihydroksybenzen, efekt doświadczenia byłby
| A. | taki sam, | ponieważ | 1. | 1,4-dihydroksybenzen jest fenolem |
| B. | inny, | 2. | w cząsteczce 1,4-dihydroksybenzenu są dwie grupy hydroksylowe. |
Schemat punktowania
1 p. – za poprawne uzupełnienie zdania przy poprawnym wyborze i zaznaczeniu odczynnika w zadaniu 21.1.
0 p. – za odpowiedź niepoprawną albo brak odpowiedzi.
Poprawna odpowiedź
B1
Zadanie 22. CKE Maj 2019 PR (formuła 2015-2022)
Jedną z metod otrzymywania halogenoalkanów jest reakcja alkoholu alifatycznego z halogenkiem fosforu(III). Ta reakcja przebiega zgodnie z poniższym schematem, w którym R oznacza grupę alkilową, a X – atom halogenu.
3R–OH + PX3 → 3R–X + H3PO3
Na podstawie: K.-H. Lautenschläger, W. Schröter, A. Wanninger,
Nowoczesne kompendium chemii, Warszawa 2007.
Napisz równanie reakcji otrzymywania 3-bromo-3-metyloheksanu opisaną metodą. Zastosuj wzory półstrukturalne (grupowe) reagentów organicznych. Napisz nazwę systematyczną użytego alkoholu.
Równanie reakcji:
……………………………………………………………………………………………………..
Nazwa systematyczna alkoholu:
……………………………………………………………………………………………………..
Schemat punktowania
1 p. – za poprawne napisanie równania reakcji z zastosowaniem wzorów półstrukturalnych (grupowych) reagentów organicznych i poprawne podanie nazwy systematycznej alkoholu.
0 p. – za odpowiedź niepełną lub niepoprawną albo brak odpowiedzi.
Poprawna odpowiedź
Równanie reakcji:
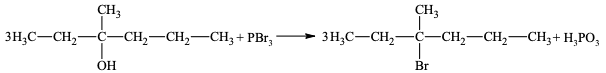
lub
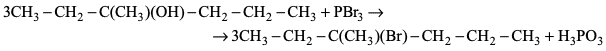
Nazwa systematyczna alkoholu: 3-metyloheksan-3-ol
Zadanie 22. CKE Czerwiec 2019 PR (formuła 2015-2022)
Do probówek, zawierających przygotowany wcześniej odczynnik, wprowadzono dwa różne związki: do probówki I – propan-2-ol, a do probówki II – propano-1,2-diol. Zawartość każdej probówki wymieszano. Objawy reakcji zaobserwowano tylko w jednej probówce.
Napisz, jaka różnica w budowie cząsteczek badanych alkoholi była przyczyną różnicy w przebiegu doświadczenia. Odnieś się do struktury cząsteczek obu związków.
……………………………………………………………………………………………………………
……………………………………………………………………………………………………………
Schemat punktowania
1 p. – za poprawne wskazanie różnicy w budowie cząsteczek obu alkoholi przy poprawnym wyborze i zaznaczeniu odczynnika w zadaniu 21.1.
0 p. – za odpowiedź niepełną lub niepoprawną albo brak odpowiedzi.
Poprawna odpowiedź
Obecność grup hydroksylowych (przy sąsiednich atomach węgla) w cząsteczce propano-1,2-diolu i jednej grupy hydroksylowej w cząsteczce propan-2-olu.
